高压放大器行业应用分享:可用于评估干细胞修复缺血性卒中潜能的神经血管芯片
微流控技术是一种通过微小的通道和微型装置对流体进行精确操控和分析的技术。它是现代医学技术发展过程中的一种重要的生物医学工程技术,具有广泛的应用前景和重要性。它在高通量分析、个性化医疗、细胞筛选等方面有着巨大的潜力,Aigtek88858cc永利官网今天就将为大家分享一篇微流控领域研究成果,一起接着往下看吧~
缺血性脑卒中是由于大脑供血不足导致神经功能的缺失。它包括炎症和免疫、细胞的死亡和分化、缺氧、血管损伤和大脑微环境改变等一系列的时空事件。干细胞治疗在动物实验和临床试点研究的支持下,已成为中风治疗的一个新兴方式。每种干细胞都有独特的特性和再生潜力,但是目前还缺乏一个可靠的中风模型来系统地比较各种候选细胞类型的疗效,并研究干细胞治疗的潜在机制。动物模型在时间和成本效率上也有固有的局限性,无法成为表征多种干细胞类型对中风引起的整个病理事件级联的治疗潜力的理想实验平台。
近期,斯坦福大学医学院神经外科的Wonjae Lee团队在Nature Biomedical Engineering上发表了题为A neurovascular-unit-on-a-chip for the evaluation of the restorative potential of stem cell therapies for ischaemic stroke的文章,利用微流控芯片技术开发了一个具有神经血管(NVU)的中风微生理系统,可用于检测干细胞治疗的神经恢复能力。此种中风模型使用人源细胞,并有一个类似于体内的3D微环境,能重现治疗用干细胞和NVU宿主细胞之间的相互作用。他们还使用该模型系统地分析了目前用于治疗中风的各类干细胞的神经恢复能力。
干细胞移植到缺血大脑的治疗效果主要取决于神经血管单元的反应。研究人员报告的适用性功能神经血管单元的微流控芯片作为微生理缺血性中风模型,概括了血脑屏障的功能,以及治疗性干细胞和宿主细胞之间的相互作用(人脑微血管内皮细胞、周星形胶质细胞、小胶质细胞和神经元)。研究人员使用该模型来跟踪一些干细胞的浸润,并描述与卒中后病理相关的基因表达水平。他们观察到,每种类型的干细胞都显示出独特的神经恢复作用,主要是通过支持内源性恢复而不是通过直接的细胞置换,突触活动的恢复与神经血管单元的结构和功能完整性的恢复有关,而与神经元的再生无关。

图1在微流控芯片中重建的脑血管屏障(BBB)的表征。A.物理屏障。芯片设计原理图(i).培养方案(ii).(NEM/AM,神经扩张培养基和星形细胞培养基的混合。NDM/AM,神经分化培养基与星形细胞培养基混合。ECM/PM,内皮细胞培养基和周细胞培养基的混合物。)神经细胞包括神经元、星形胶质细胞和小胶质细胞,其最终比例预计为8:4:1。血管细胞包括内皮细胞和周细胞,比例为9:1。芯片中NVU组成细胞的空间分布(iii)。明场图像显示水凝胶(蓝色)部署在脑通道(iv)。相位对比(v)和荧光(vi)图像显示血侧(左)通道和脑(右)通道之间清晰的边界(白色箭头)。分别用抗cd31和抗gfap抗体对内皮细胞和星形胶质细胞进行染色。形成的内皮层阻止了绿色荧光探针(FITC右旋糖酐,4kda)在其上的自由扩散(vii)。加入探针1小时后拍摄图像。单层共聚焦显微镜图像显示水凝胶侧壁形成的内皮细胞(viii)。内皮细胞进行VWF染色。共聚焦显微镜图像的三维重建视图显示均匀的内皮细胞(ix)。内皮细胞和星形胶质细胞分别进行了特异性标记CD31和GFAP染色。切片中内皮细胞表观渗透性系数Papp的对数变换值(n=5)(x)。B.生物化学屏障。血侧通道含血清培养基和脑脊液侧通道无血清培养基混合培养条件示意图(i)。在无内皮细胞(白色箭头表示水凝胶边界)的样品中,小胶质细胞(IBA-1染色为绿色)显示CD68表达上调(红色),在有重建内皮细胞的样本中,大部分小胶质细胞不表达CD68(iii)。有内皮细胞和没有内皮细胞的样本之间的CD68表达(n=3)(iv)。C.细胞选择障碍。癌细胞合并示意图(i)。将两种人乳腺癌细胞系MB-231和MB-231Br的预染色细胞注入血侧通道。MB-231(ii)和MB-231Br(iii)的荧光图像在注射后3d拍摄。白色箭头表示水凝胶边界。测量了血脑屏障外渗的程度(n=3)。
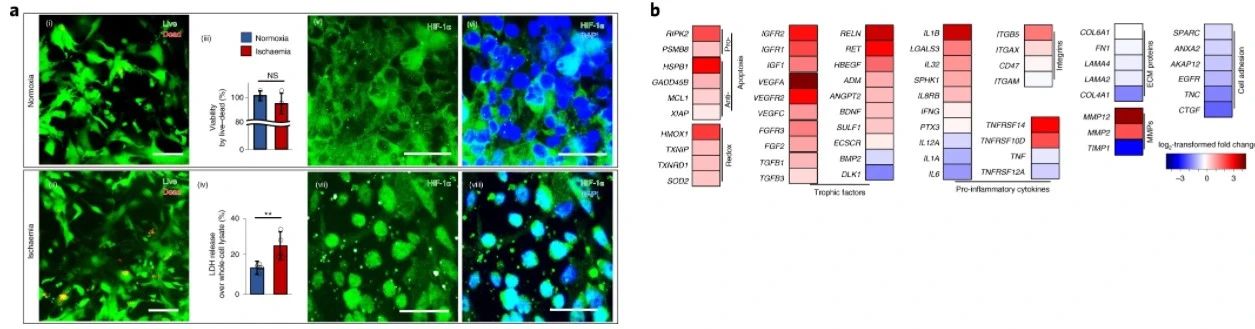
图2缺血模型建立。A.活/死检测:在常氧(i)和缺血(ii)条件下,活细胞用钙黄素染色为绿色,死细胞用乙二胺(EthD-1)染色为红色。使用活/死测定法定量测定生存能力(n=3)(iii)。通过细胞外LDH水平测定细胞毒性(n=5)(iv)。在缺氧时,HIF-1α主要位于胞浆(v和vi),在缺血时,HIF-1α聚集在细胞核(vii和viii)。B.缺血引起的基因表达变化。

图片图3神经元、内皮细胞和周细胞行为。A.神经元的行为。常氧样本中神经元的相位对比图像(i)。白色箭头表示水凝胶边界。来自hiPSCs的神经元表达成熟的神经元标记物MAP-2和突触素I和II(SYN)。对NVU细胞成分进行神经元标记物MAP-2和星形细胞标记物GFAP的免疫染色。几乎没有彩色的神经元(iv)。Fluoro-JadeC染色神经元缺氧(vi)。基因表达改变的缺血(vii)。分化NPCs(viii至xiii)中胞浆钙离子(Ca2+)的自发振荡。NPCs用DiL(红色)预染色。采用fluo-4am(绿色)检测细胞内Ca2+浓度。从4个独立的样本中随机选择表达il的细胞,在缺氧状态(n=34个细胞)和缺血状态(n=14个细胞)各2个。分化后的NPCs在10min内表现出4种不同的Ca2+振荡模式(ix),标记的细胞分别表现出振荡模式、瞬变模式、持续模式和不明显模式。为每个Ca2+细胞的比例数字振荡模式(x)和细胞数量的变化(xi)。由于缺血细胞钙振荡的振幅和频率显示振荡Ca2+信号。B.内皮的行为。荧光(i和iii)和相位对比(ii和iv)图像显示有或没有流动的内皮形态。ZO-1和VEGF表达遍布于缺血的内皮。ZO-1表达的整体程度内皮通过引入流量增加和减少在缺血性疾病(n=3)(vi)。ZO-1表达式的空间分布在单个细胞量化通过计算像素的数量(y轴)相应的荧光强度(x轴)。ZO-1表达式在缺血性细胞分散在整个胞体与局部峰值的模式显示在常氧细胞。内皮在缺血时上调VEGF表达(n=3)(ix)。C.周细胞的行为。少量周细胞暴露在内皮(i)和脑通道(ii)侧壁之间。白色箭头表示周细胞。

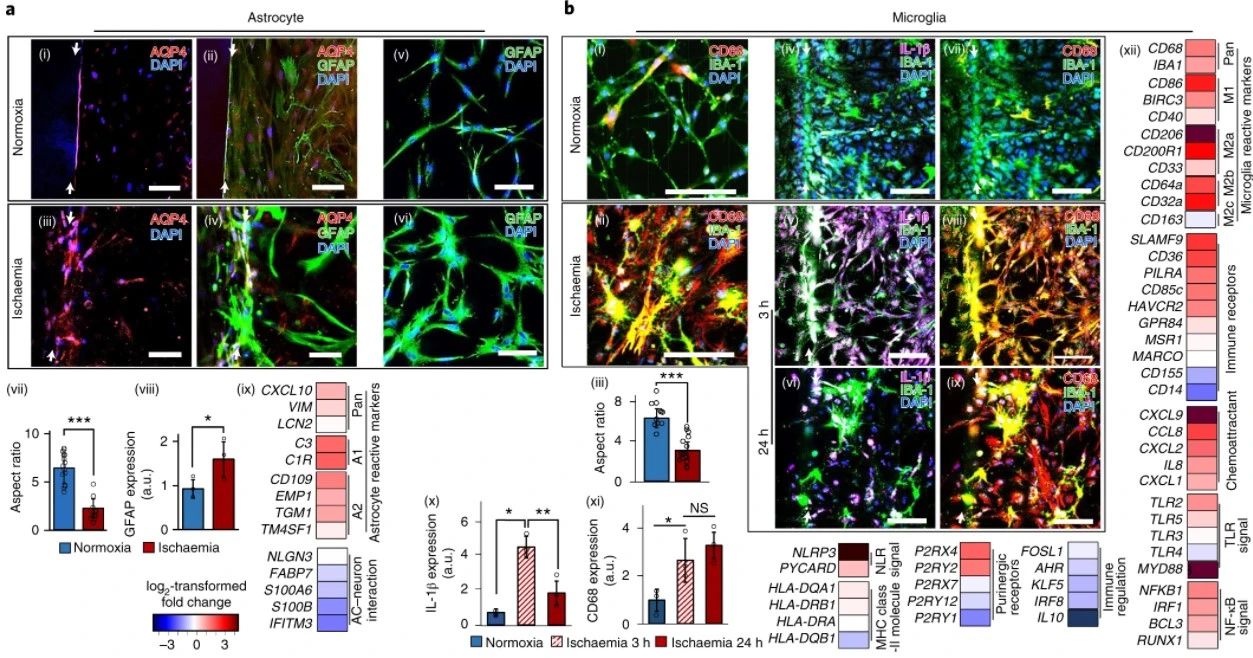
图4星形胶质细胞和小胶质细胞行为。A.星形胶质细胞的行为。常氧星形胶质细胞中的AQP4定位于水凝胶侧壁形成的内皮(i和ii),而缺血星形胶质细胞中的AQP4分布于胞体(iii和iv)。常氧(v)和缺血(vi)星形胶质细胞中GFAP的表达。在常氧和缺血样本中,星形细胞胞体的最长和最短轴的比值(vii)。分析了来自3个独立芯片的15个细胞。定量的星形胶质细胞GFAP在常氧和缺血样本中的表达水平(n=3)(viii)。B.小胶质细胞的行为。缺血时小胶质细胞(用抗iba-1抗体染色)上调CD68的表达(i和ii)。正常氧和缺血样本中小胶质细胞体的最长轴和最短轴的比值(iii)。小胶质的表达il-1β和CD68在常氧和缺血性(3h和24h)样品.小胶质细胞移植的表达il-1β只在最初几个小时的局部贫血的发病.CD68在整个时间缺血小胶质细胞中表达(n=3)(xi)。
该研究概述了体外正常和缺血条件下的NVU行为,从而有效和系统地评估干细胞治疗的疗效,克服了动物模型和目前可用的体外模型的局限性。这项研究的结果,特别是不同干细胞的神经恢复潜力的特征,可以在研究和临床中引导干细胞治疗的方向。这项工作中提出的方法也立即适用于广泛的其他脉管系统相关疾病,在精准医疗领域开辟了新的可能性。

带宽:(-3dB)DC~200kHz
电压:800Vp-p(±400Vp)
电流:40mAp
功率:16Wp
压摆率:≥356V/μs
可程控
参考文献
Lyu, Z., Park, J., Kim, KM. et al. A neurovascular-unit-on-a-chip for the evaluation of the restorative potential of stem cell therapies for ischaemic stroke. Nat Biomed Eng 5, 847–863 (2021).
西安88858cc永利官网是专业从事功率放大器、高压放大器、功率信号源、前置微小信号放大器、高精度电压源、高精度电流源等电子测量仪器研发、生产和销售的高科技企业,为用户提供具有竞争力的测试方案。Aigtek已经成为在业界拥有广泛产品线,且具有相当规模的仪器设备供应商,样机都支持免费试用。如想了解更多功率放大器等产品,请持续关注88858cc永利官网官网www.aigtek.com或拨打029-88865020。
原文链接:/news/2490.html